폐암 진단 및 추적을 위한 자동화 RECIST 기술 with Multi-Time Point Segmentation
포스트 코로나 이후 최근까지 폐 건강에 대한 관심이 크게 증가하고 있습니다. 이러한 현상은 폐암, 만성 폐쇄성 폐 질환(COPD), 천식, 폐 섬유증과 같은 폐 관련 질환의 증가와 밀접하게 관련되어 있습니다. 폐 질환의 증가는 전 세계적으로 수많은 사망 원인과 장기적인 건강 문제를 발생시키고 있습니다. 이에 따라 폐 건강에 대한 연구와 치료 개발에 대한 필요성이 점점 강조되고 있습니다.
저희 테서는 폐 질환 문제를 해결하기 위해서 폐암 추적 알고리즘을 도입한 자동화 RECIST 분석 툴을 개발하였습니다. 본 글은 저희가 AI 모델을 활용하여 폐 종양을 추적 관찰 기술과 RECIST 1.0, RECIST1.1 알고리즘으로 수동으로 진행하는 폐 질환 진단 과정을 자동화하는 기술에 대한 내용입니다.
배경
폐암과 만성 폐 질환은 전 세계적으로 중요한 건강 문제입니다. 이에 따라, 폐 건강을 개선하기 위한 새로운 치료법과 기술의 개발에 의료계가 집중하고 있습니다. 폐암의 경우 전 세계적으로 흔한 암으로, 많은 연구가 진행되고 있는 중입니다. 이 과정에서 RECIST 기준은 폐암 치료의 효과를 객관적으로 평가하는 중요한 도구입니다.
RECIST는 암 치료 반응을 평가하는 국제 기준입니다. 이를 통해 폐암을 포함한 종양에 대한 치료의 효과를 일관되고 정확하게 평가할 수 있습니다. 또한 RECIST 기준을 통해서 새로운 치료법의 효과를 객관적으로 측정하여, 기존 치료법과 비교할 수 있습니다. 다양한 국가와 기관 간의 임상 연구 결과를 비교하는데 큰 도움이 됩니다.
그러나 RECIST 기준을 적용하고자 종양 일일이 캘리퍼로 측정해야 되기 때문에, 환자 한명 당 소요되는 시간 오래 걸려 비효율입니다. 또한 전문의에 따라 기준이 조금씩 다르기 때문에 일관되지 않은 결과를 도출할 확률이 높습니다.
저희 테서는 종양의 위치 탐지와 종양 측정의 일관성 문제를 해결하기 위해서 인공지능을 활용한 자동화된 RECIST 기술을 개발 하였습니다. 자동화된 RECIST 기술은 데이터 기반 접근을 통해 암 치료의 최적화 및 일관성을 도모하고, 분석에 들어가는 시간과 비용을 절감할 수 있습니다.
RECIST 기술은 네 가지 주요 파트로 구성되어 있습니다.
첫 번째는 폐 종양의 위치를 찾기 위한 ‘폐 종양 분할 모델’입니다. 이 segmentation 기술을 통해 CT 영상에서 폐 종양을 높은 성능으로 추출합니다.
두 번째는 치료 경과 비교를 위해 서로 다른 시점에 촬영된 CT 영상들의 위치를 보정해주는 ‘폐 정합 모델’입니다. 이는 시간에 따라 변화하는 폐의 형태와 위치를 고려하며, 종양의 변화를 좀 더 명확하게 관찰 할 수 있게 해줍니다.
세 번째는 서로 다른 영상에서 같은 종양인지 판단하는 ‘폐 종양 추적 알고리즘’입니다. 이는 종양의 성장률과 RECIST를 평가하는데 중요한 정보를 제공합니다.
마지막으로 RECIST 1.0과 RECIST 1.1 기준에 따른 판단을 내려주는 ‘RECIST 판단 알고리즘’이 포함됩니다. 이 알고리즘은 종양의 크기 변화를 기준으로 치료의 효과를 객관적으로 평가하고, 환자의 치료 계획을 조정하는데 도움이 됩니다.
1. 폐 종양 분할 모델 학습
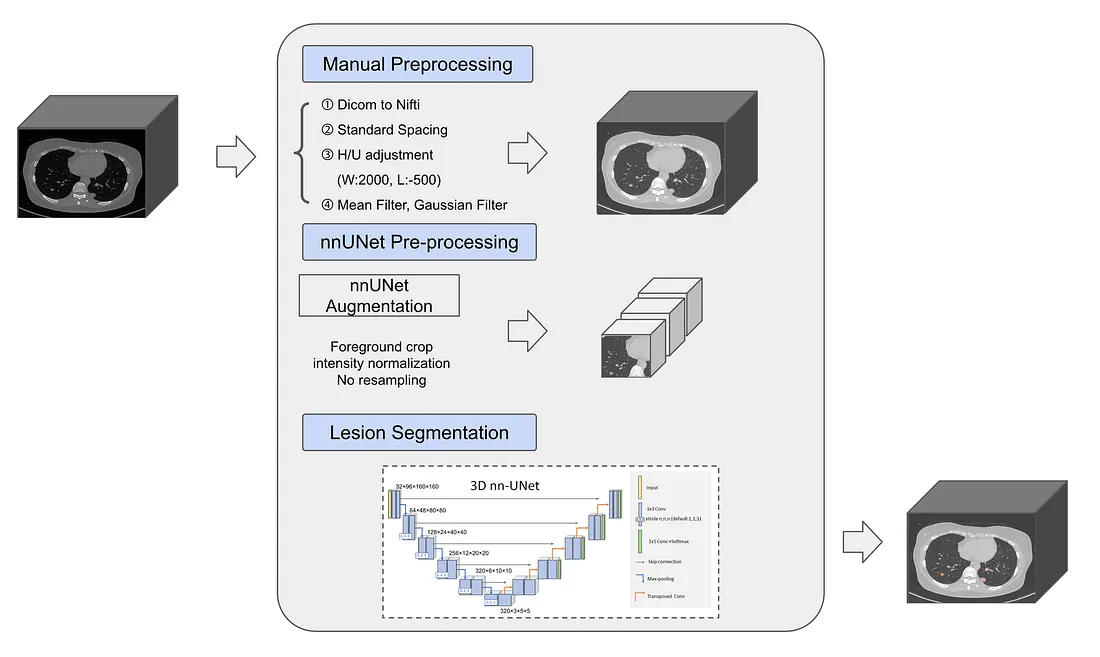
우선 폐 종양의 위치를 찾기 위해서는 폐 종양 분할 모델이 필요합니다. 임상 환경에서의 Lung CT 데이터의 경우 modality마다 특성이 매우 다르고 3D 데이터에서 각 이미지마다 pixel의 distance의 특성이 다르다는 어려움이 존재합니다. 이를 해결하기 위해 병원 환경에 따라 편차가 크게 존재하는 데이터에서도 다양한 augmentation과 pre processing 기법을 적용하여 이를 해결하고자한 nnUNet을 채택하였습니다.
해당 모델을 사용하여 각 modality, dataset마다 데이터의 특성에 맞게 custom engineering 및 학습을 진행했습니다. 폐 종양을 수월하게 찾기 위해서 폐의 Hounsfield units에 맞게 CT 데이터의 window level과 window width를 조절하는 전처리 후 폐 종양 분할을 진행 했습니다.
2. 폐 정합 모델 학습
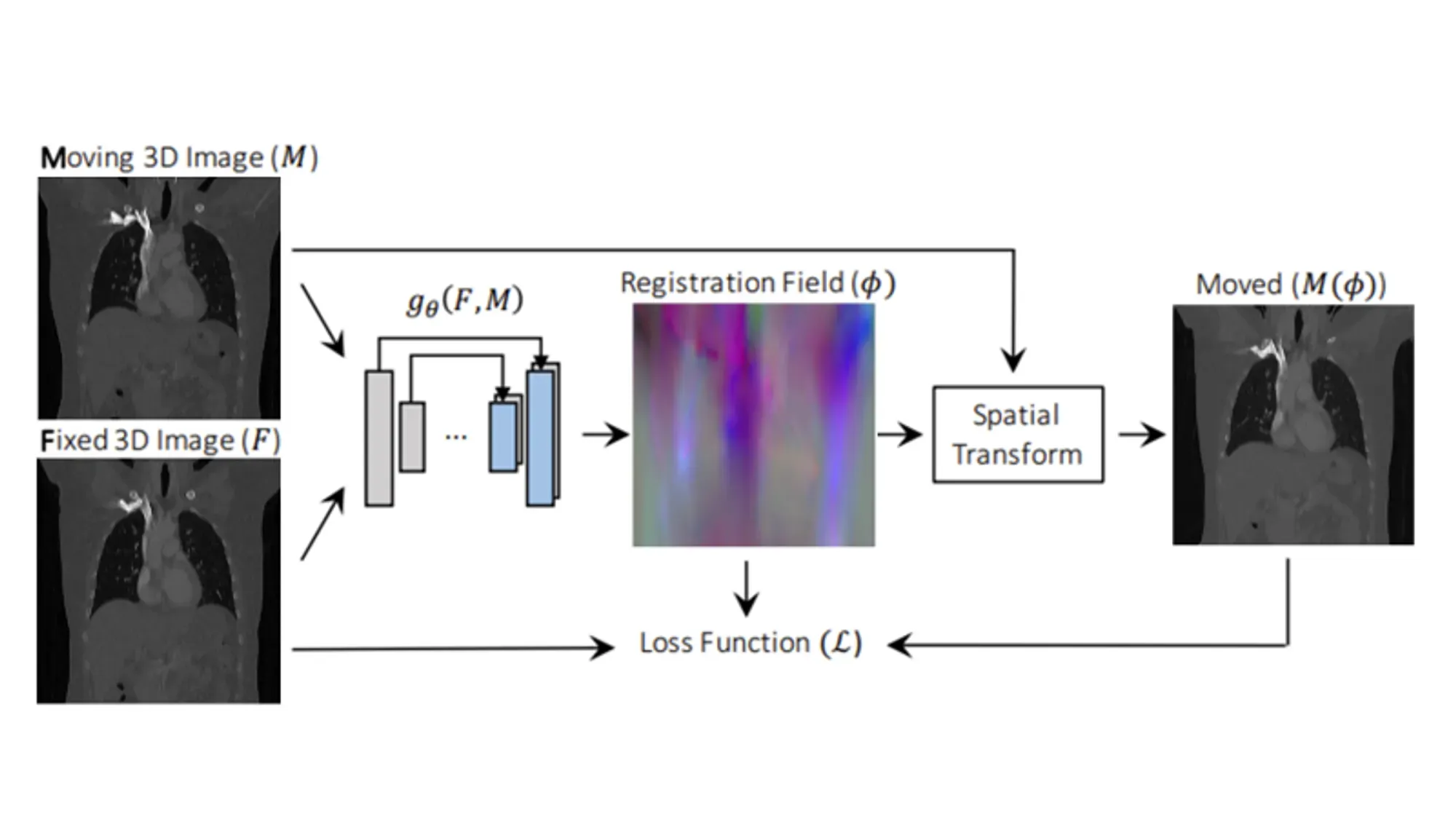
환자의 치료 경과를 확인하기 위해서 서로 다른 시점에 촬영된 CT 영상을 Baseline CT에 맞추는(align) 과정이 필요합니다. 영상을 정합하는 이유는 각 영상마다 종양의 위치 및 크기가 다르기 때문에 같은 종양을 맞추는 과정이 필요하기 때문입니다. 현재 의료 영상 정합 모델 중 최고의 성능을 내고 있는 모델인 VoxelMorph를 기반으로 모델을 개발하였습니다.
VoxelMorph란 의료 영상 분야에서 사용 되는 딥 러닝 기반의 이미지 정합 알고리즘입니다. VoxelMorph는 신경망을 통해 영상 간의 변환 매핑을 학습하며, 이를 통해 빠르게 정확한 영상 정합을 가능하게 합니다.
위 VoxelMorph 모델의 기본 구조에서 중앙에 위치해있는 Registration Field는 정합할 대상 이미지와 기준이 되는 이미지 사이의 Vector Map 입니다. 벡터맵에는 얼마나 이동해야 되는지에 대한 정보가 포함되어 있습니다. Spatial Transformer에 Registration Field와 정합할 대상 이미가 들어가게 되면 Registration Field의 값만큼 이동한 정합 이미지가 생성되게 됩니다.
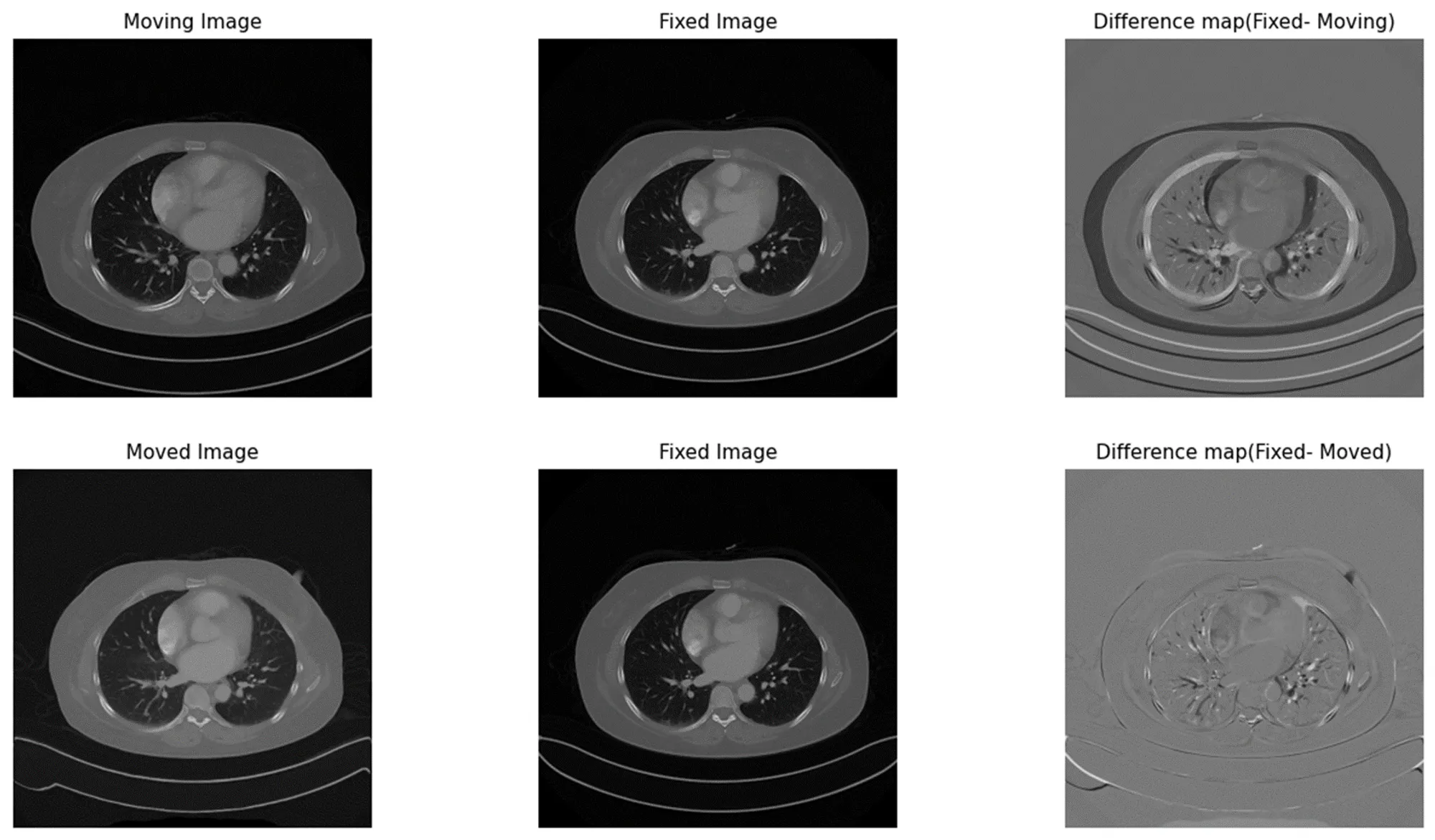
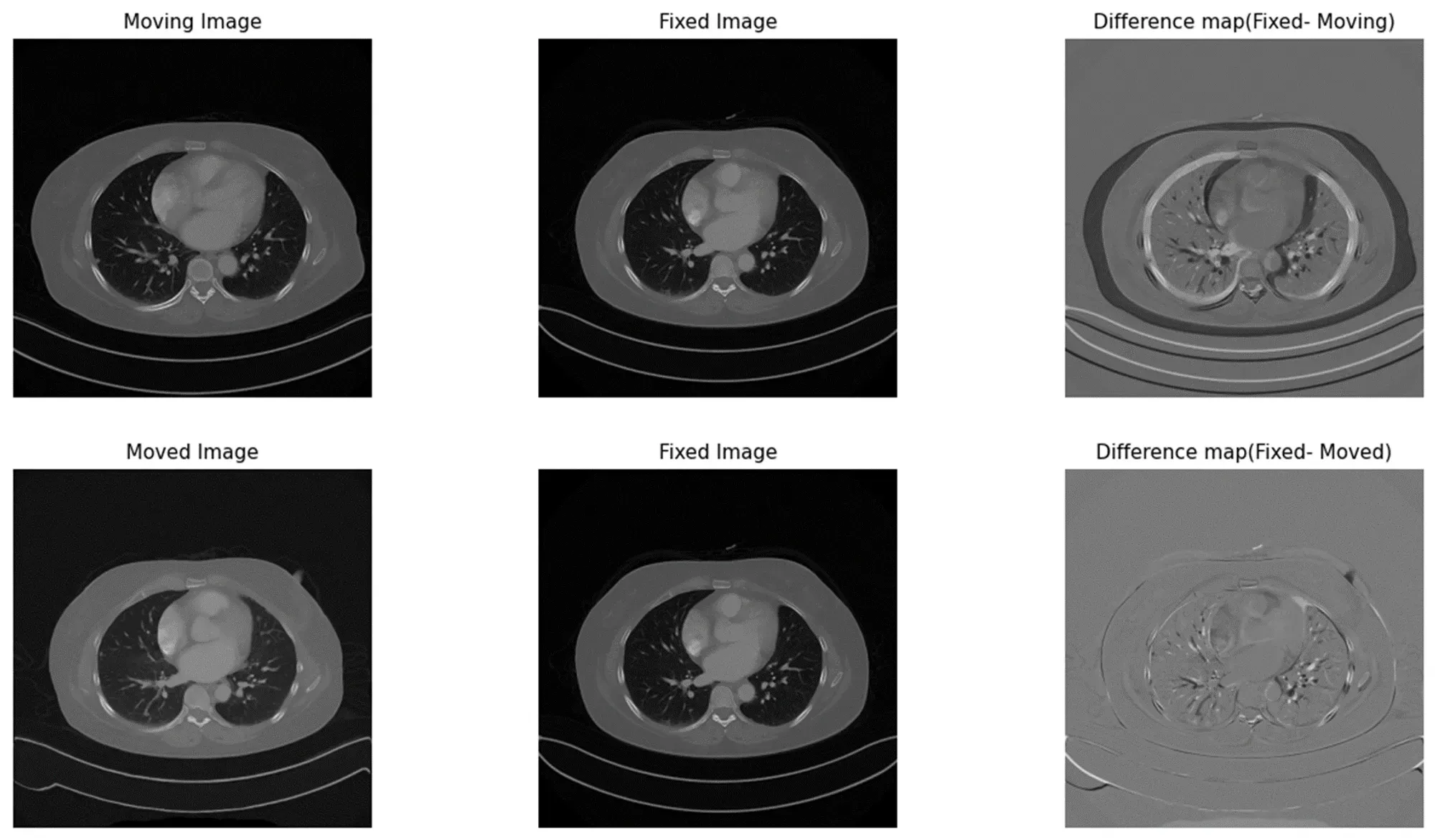
CT 데이터의 크기가 상당히 크기 때문에, 효율적인 학습을 위해서 Patch 기반으로 접근 방식을 채택하였습니다. 위 그림의 경우 폐 정합 모델을 통해서 정합 대상 이미지가 정합된 이미지가 된 결과입니다.
상단 가장 오른쪽에 위치해있는 Difference map을 보게 되면 정합되기 이전인 정합 대상 이미지와 정합 기준 이미지 간의 폐의 크기와 바깥 몸의 부피 위치 차가 상당히 크게 나는 것을 확인 할 수 있습니다.
하지만 하단의 가장 오른쪽 위치해있는 Difference map을 확인하면, 크기와 몸의 부피의 차이가 확연하게 줄어든 것을 확인 할 수 있습니다.
3. 폐 종양 매칭 알고리즘
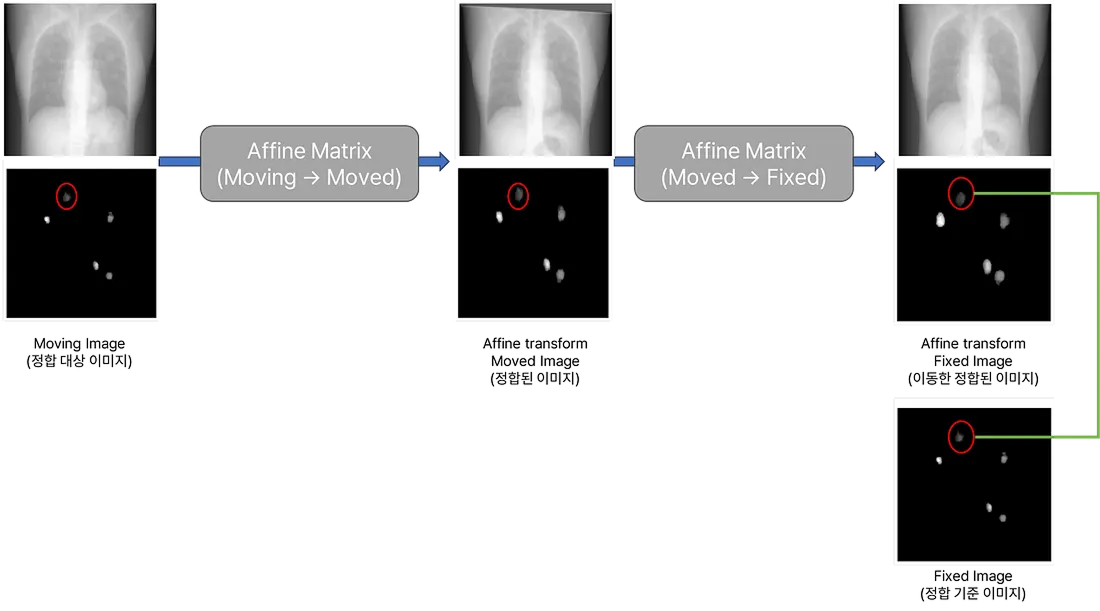
VoxelMorph를 통해 정합이 완료 되었다면 Moving Image(정합 대상 이미지), Fixed Image(정합 기준 이미지), Moved Image(정합된 이미지) 영상들이 생성됩니다. 위 그림에서 위 폐 사진은 이미지로 지칭하고, 아래 종양 사진은 이미지의 종양 정보라고 지칭하겠습니다.
우선 동일한 종양을 매칭하기 위해 각 세 영상 간의 이동 정보가 담긴 Affine Matrix를 구합니다. 그 이후에 Segmentation을 통해 생성된 각각의 종양 영상에 아래와 같은 과정을 수행합니다.
- Moving -> Moved Affine Matrix를 이용하여 정합 대상 이미지의 종양 정보를 정합된 이미지의 종양 정보로 Transform 합니다.
- Moved -> Fixed Affine Matrix 정합된 이미지의 종양 정보를 이동한 정합된 이미지의 종양 정보로 Transform 합니다.
위 과정이 진행된 이후에는 정합 기준 이미지의 종양 정보와 이동한 정합된 이미지의 종양 정보를 비교하여 각 종양이 동일한 것 인지를 판단합니다. 이때, 종양의 위치와 부피 정보가 중요한 요소로 작용합니다. 따라서, 이러한 정보들을 고려하여 Cross correlation 공식을 사용하여 종양이 동일한지 여부를 결정합니다.
4. RECIST 판단 알고리즘
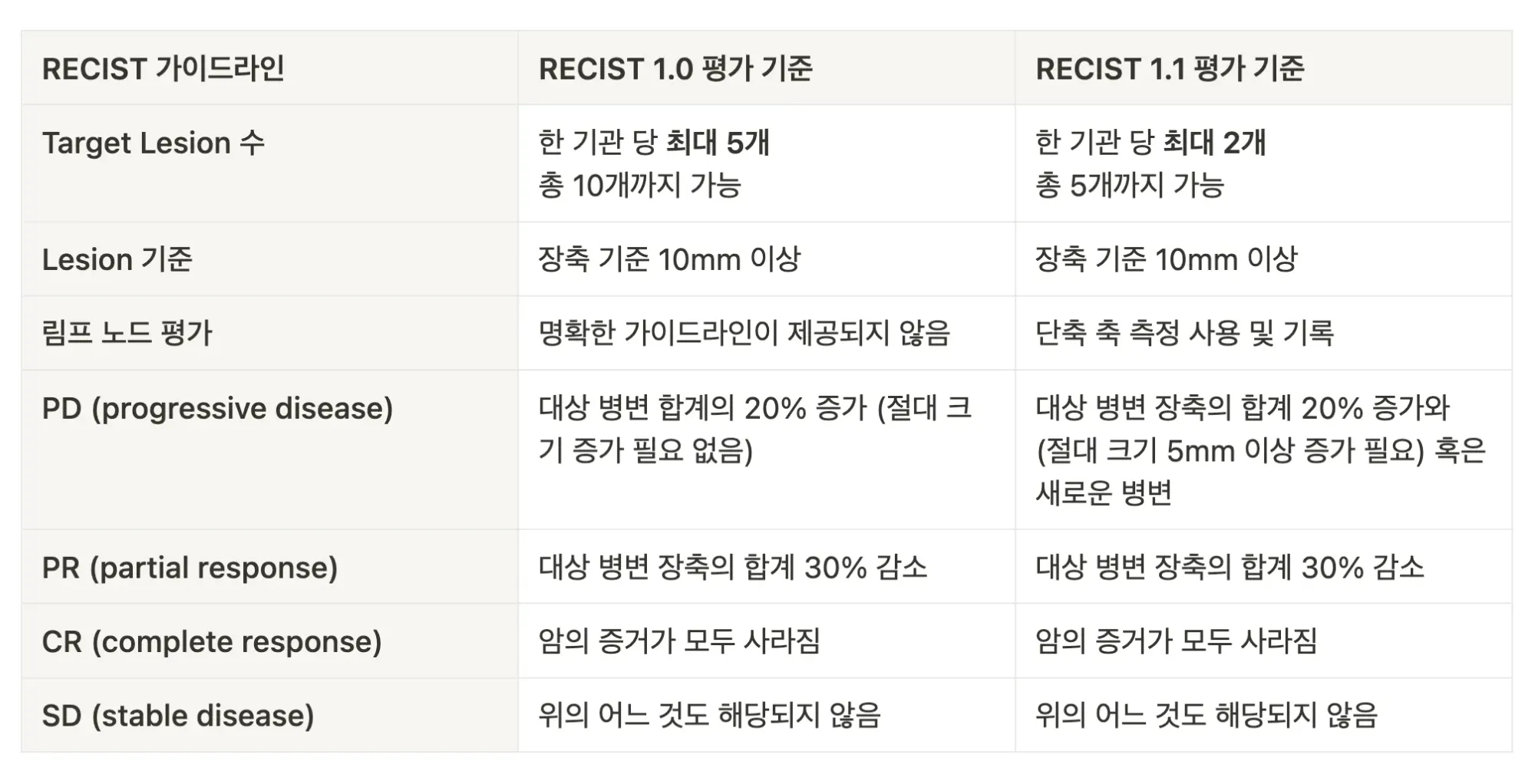
위의 표는 국제 표준 기준인 RECIST 1.0과 RECIST 1.1을 비교한 표입니다. RECIST 1.1의 경우 RECIST 1.0에 비해 측정하는 종양의 수가 줄어든 점이 가장 큰 차이였습니다. 또한 부분 반응(Partial Response)과 질병 진행(Disease Progression)의 기준을 조정해서 최소로 증가해야되는 절대 크기 기준이 추가가 되었습니다.
폐 종양 매칭 알고리즘을 통해 매칭된 폐 종양들의 크기 변화를 종합적으로 분석하였습니다. 분석된 결과를 토대로 RECIST 기준에 따른 판단을 진행했습니다. RECIST 판단 알고리즘은 종양의 크기 변화를 정밀하게 측정하여 RECIST 기준을 효과적으로 적용할 수 있도록 합니다.
최종적으로 PR, PD, SD, CR를 분류한 결과 Accuracy 91.1%이라는 높은 성능을 달성하였습니다.
마치며
이번 프로젝트를 통해 폐암 진단 및 추적에 있어서 인공지능의 중요성과 가능성을 다시 한번 확인할 수 있었습니다. 자동화 RECIST 기술의 개발은 폐암 치료 과정에서의 정밀한 모니터링과 효과적인 치료 계획 수립에 큰 도움을 줄 것으로 기대됩니다. 특히, RECIST 기준에 따른 자동화된 평가는 의료 전문가들에게 시간적, 물리적 부담을 줄여주며, 더욱 일관된 결과를 제공합니다.
이 기술은 단순히 폐 질환에만 국한되지 않고, 다양한 암 종류와 만성 질환의 추적 및 평가에도 응용될 수 있는 확장성을 가지고 있습니다. 이를 통해 환자 맞춤형 치료 계획의 정확성을 높이고, 장기적으로는 환자의 생존율 향상에 기여할 수 있을 것입니다. 이는 결국 의료 서비스의 질을 높이는 데 기여하며, 앞으로도 저희 테서는 지속적인 연구와 개발을 통해 의료 분야의 혁신을 이끌어 나갈 것입니다.


